2026.04.02
在新药研发进程中,药物性肝损伤(DILI)和胃肠毒性是导致候选药物研发失败的核心因素。行业数据显示:药物从Ⅰ期临床到最终获批上市的成功率仅8%,其中安全性相关问题占研发失败原因的比例高达59%。传统毒理学评价依赖动物模型和二维(2D)细胞培养,存在显著局限:2D 单层细胞会在数天内丧失关键代谢功能,易产生假阳性或假阴性结果,既可能误判安全分子,也可能放行高风险化合物进入临床。
2025年4月,美国FDA 发布逐步淘汰动物试验的路线图,明确将基于人类原代细胞的新方法学(NAMs)从研发中的 “可选补充手段” 升级为药品监管层面的 “刚需技术”。美国 VivoSim 公司推出 NAMkind™ 毒理学平台,该平台依托专利化的人源 3D 肝脏与肠道模型,可有效弥补传统药物评价模型的技术局限,为药物研发提供高度贴合人体生理特征、可靠性强的安全数据,为小分子、抗体药物偶联物(ADC)等多模态药物的管线研发保驾护航,助力优质候选药物高效推进研发进程。
NAMkind™平台:体外重构功能性人源肝肠组织,真实还原生理毒性应答
NAMkind™平台突破传统动物实验与简化细胞体系的技术局限,依托专利多细胞共培养技术,以健康供体来源的人原代肝细胞、肠上皮细胞、平滑肌细胞、成纤维细胞及内皮细胞为原材料,构建出具备完整生理结构与功能的3D微组织模型。该模型可稳定培养7~21天,能精准模拟药物在人体内的长期暴露模式与联合用药场景。
NAMkind™ 肝脏模型:精准捕捉 DILI 风险
NAMkind™肝脏模型采用肝细胞、Kupffer 细胞、肝星状细胞、内皮细胞四细胞共培养体系,高度还原人体肝脏微环境,可通过炎症、纤维化等多条通路综合评估肝毒性。模型以 ATP、LDH、白蛋白为核心检测标志物,对 DILI 的预测准确率达 91%、敏感性 88%、特异性 100%,有效排除假阳性结果干扰,降低后期研发失败风险。
NAMkind™ 肠道模型:精准评估肠道毒性与部位特异性
NAMkind™肠道模型由人原代肠上皮细胞、平滑肌细胞、成纤维细胞及内皮细胞共培养构建,具备极化上皮结构、紧密连接功能,以及功能性CYP450酶与转运蛋白体系,可稳定分泌黏蛋白,支持屏障完整性、组织活力等多维度指标检测,能够捕捉传统评价方法难以识别的腹泻、炎症等肠道毒性反应。模型提供回肠与结肠专属版本,可分区监测不同肠段的细胞活力,动态反映药物对肠道的部位特异性毒性特征,为临床剂量选择与风险管理提供关键参考数据。
服务模式:贯穿研发全周期,实现毒性风险前置与精准管控
NAMkind™毒理学服务深度匹配药物研发的核心决策节点,将肝肠毒性风险管控环节前置,覆盖研发全周期,可提供分阶段定制化服务:
1. 前瞻性筛选(Hit-to-Lead 及早期先导优化)
该服务可在2周内完成20余种化合物的筛选,通过核心生物标志物(ATP、白蛋白、LDH、TEER等)快速识别肝肠毒性信号,为化合物化学结构优化提供方向指导,助力研发团队锁定高安全性候选分子。
2. 转化风险桥接(晚期先导优化→候选物提名)
搭配物种特异性模型与机制研究矩阵,验证动物实验数据与人体生理反应的相关性,输出符合新药临床试验(IND)申报要求的安全性数据,支撑监管申报材料提交。
3. 研究性毒理学(临床 / 临床前意外毒性)
可快速重现或排除待确认的毒性信号,深入追溯毒性发生的分子机制,为项目后续推进、优化或终止的决策提供明确建议,高效实现项目价值,避免不必要的研发全线停摆。
技术实力:经临床药物验证,为研发决策提供可靠数据支撑
NAMkind™模型已通过大量经临床验证的药物全面校验,预测精度优异,不仅适用于小分子药物的毒性评估,更可对ADC等大分子药物的肝肠毒性实现精准评价,检测结果与药物临床实际表现高度吻合。
1. 小分子药物验证:精准识别结构相似化合物的差异毒性
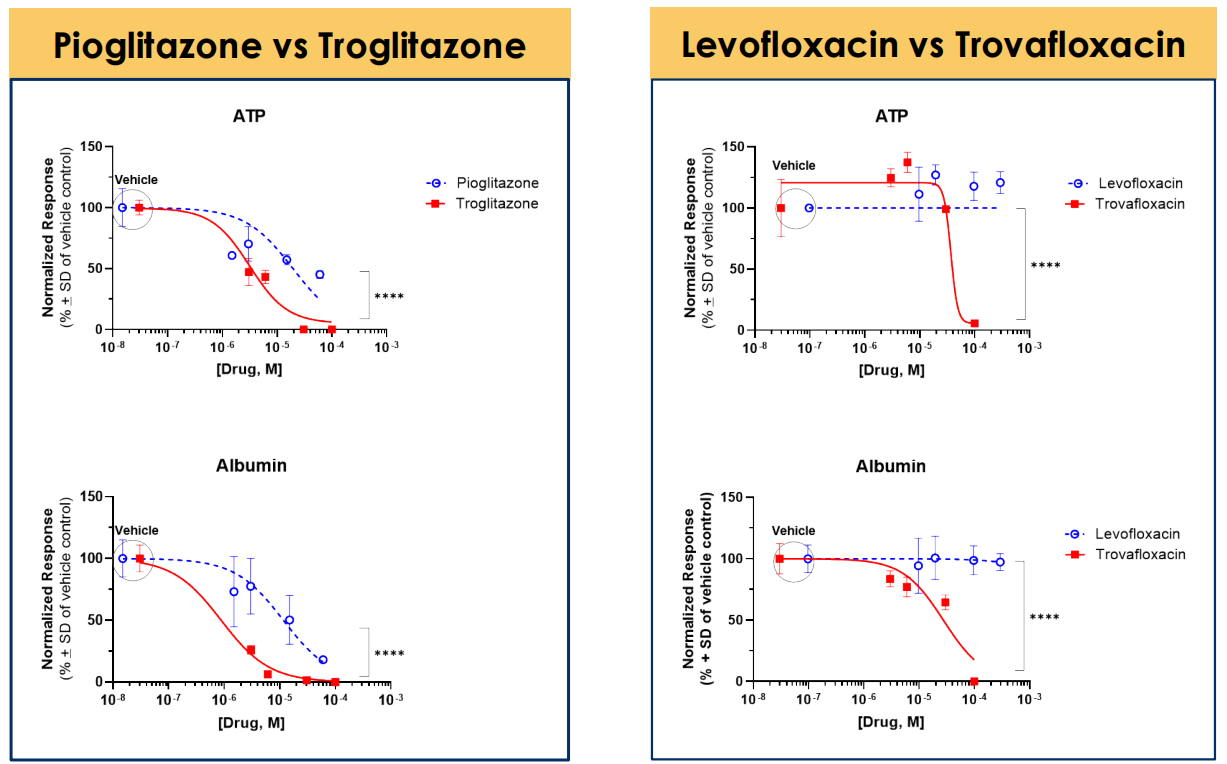
肝脏模型:因严重 DILI 撤市的曲格列酮、曲伐沙星,在模型中均表现出显著的肝细胞功能抑制,ATP 与白蛋白水平大幅下降;而其同类安全药物吡格列酮、左氧氟沙星则无明显毒性信号,该对照结果充分证明模型可精准筛选安全性更优的候选药物分子。
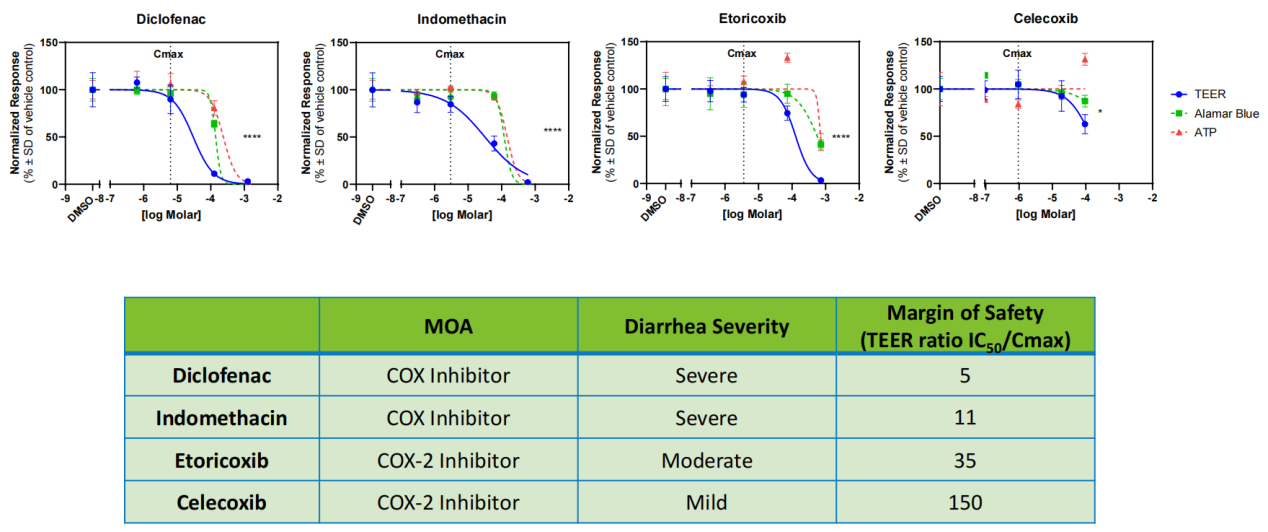
肠道模型:对非甾体抗炎药的验证显示,双氯芬酸、吲哚美辛的肠道毒性显著,安全边际值仅为5倍和11倍;而塞来昔布、依托考昔的毒性轻微,对应安全边际值分别达150倍和35倍,模型检测结果与药物临床引发的腹泻严重程度高度匹配。
2. ADC药物验证:精准区分靶向 / 脱靶毒性,针对性解决 ADC 研发中的核心安全挑战
肝脏与胃肠道是ADC类药物主要脱靶毒性器官。NAMkind™模型依托人原代细胞的天然靶点表达特征,可精准解析药物毒性作用机制。
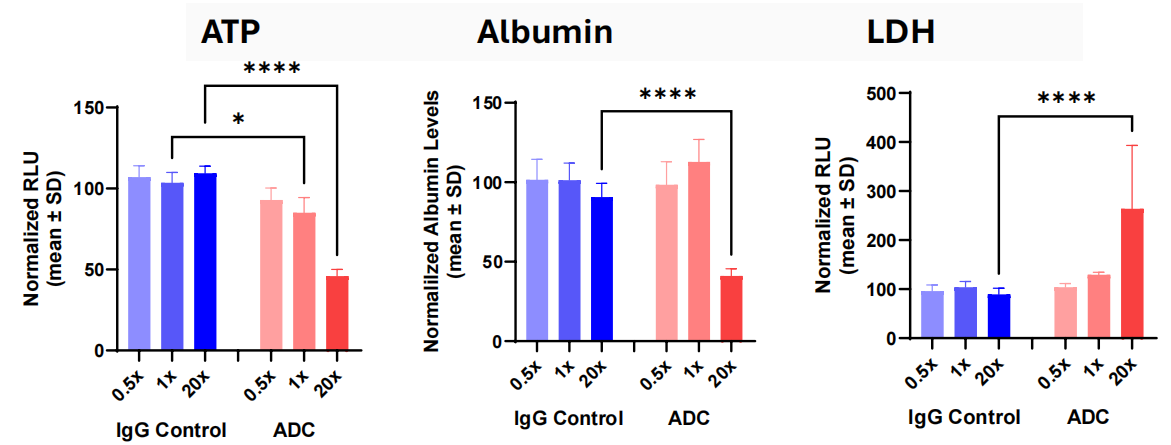
肝脏模型:针对靶向CD33的吉妥珠单抗奥佐米星开展的测试显示,因模型中内皮细胞与Kupffer细胞高表达CD33,该药物呈现出显著的剂量依赖性肝毒性,即ATP 下降、白蛋白分泌受抑和LDH 释放升高;三项核心肝毒性指标均表现出明显的剂量依赖性变化,而同亚型对照IgG无任何毒性信号。模型检测结果与该药物临床易引发肝窦阻塞综合征的肝毒性特征高度吻合,直观验证了模型能精准识别 ADC 靶点介导的肝损伤风险。
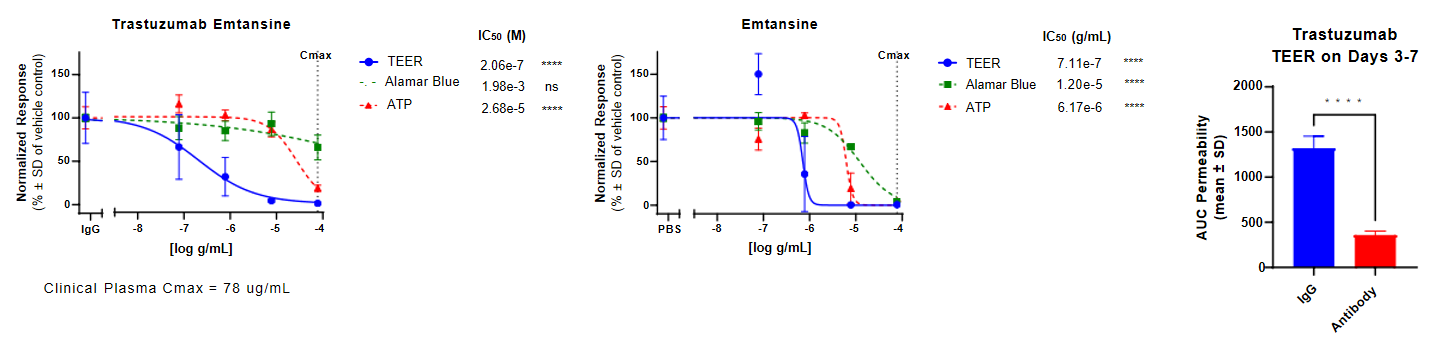
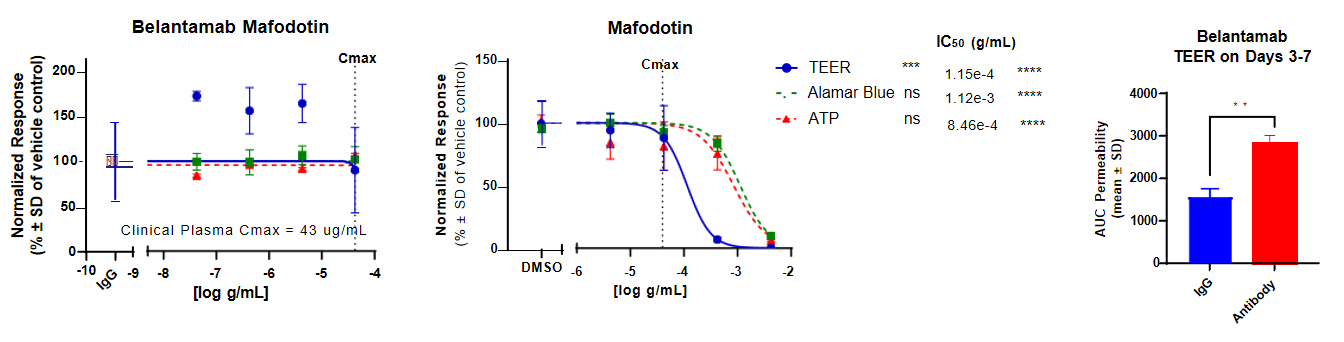
肠道模型:在NAMkind™肠道模型中对靶向HER2的ADC药物恩美曲妥珠单抗开展验证,由于模型细胞高表达该药物的作用靶点HER2,完整ADC在TEER(跨上皮电阻)、Alamar Blue(细胞活力检测)、ATP(三磷酸腺苷)三项检测指标上均呈现显著的剂量依赖性毒性;此外游离载荷也表现出毒性,未偶联的抗体单独作用即可破坏黏膜屏障,整体结果与临床中该药物引发腹泻等胃肠道不良反应高度一致,证实NAMkind™肠道模型可准确识别ADC的靶点介导的胃肠道毒性,适用于ADC早期胃肠道安全风险评估。
核心竞争优势:高预测精度与高效研发并行,赋能研发价值提升
NAMkind™凭借高精准、快周转、全合规、多模态的核心优势,成为药物毒理学评价的新一代解决方案,相较传统毒理学模型与同类产品,可为药物研发创造显著价值:
优异预测精度:肝脏模型 DILI 预测准确率达91%(特异性 100%)、肠道模型肠道毒性预测准确率达96%(敏感性 97%),可精准捕捉传统模型遗漏的人体特异性毒性信号;
高效周转效率:从接收受试化合物到出具完整机制评价报告仅需4周左右,前瞻性筛选仅需2周即可完成,较常规动物实验(4-6个月)提速数倍,抢占研发窗口期;
大幅降本增效:临床前筛除 1 个高毒性候选化合物,可避免后期数亿美元的研发损失,目标将毒性导致的临床失败率降低 50%,性价比远超动物实验;
全球监管认可:完全符合FDA NAMs规范,同步适配NMPA、EMA的监管要求,符合国际申报标准,输出的监管级数据可直接支撑IND申报,有效提升申报成功率;
ADC专项能力:可精准区分ADC靶向/脱靶毒性,解析连接子类型、DAR 值对毒性的影响,针对性解决国内ADC研发面临的关键安全问题,为海外授权与出海提供合规数据支撑;
全流程覆盖能力:可覆盖从苗头化合物筛选、先导化合物优化,到候选化合物(PCC)提名、IND申报,再到临床阶段意外毒性溯源研究的全链路环节,可为药物研发全周期提供定制化毒理学评价服务,实现毒性风险的全流程前置管控。
NAMkind™依托高仿真人源化3D肝肠器官模型,凭借经临床验证的高预测精度,直击药物研发中肝损伤与肠道毒性两大核心安全痛点。该平台不仅填补了传统动物与细胞模型在人体毒性预测上的技术短板,更以全流程、合规化、高效率的毒理学服务,贯穿药物从早期筛选到临床申报的全研发周期。
未来,NAMkind™ 将持续赋为小分子、ADC等多模态创新药研发赋能,有效降低临床失败风险、压缩研发周期、节约研发成本,助力中国创新药合规出海、高效落地,推动更多安全可靠的候选药物早日实现转化上市。




