2026.03.26
雌激素受体阳性(ER+)乳腺癌约占全部乳腺癌病例的70%,其侵袭转移是导致患者死亡的主要因素。尽管内分泌治疗显著改善了ER+乳腺癌患者的预后,但治疗过程中出现的获得性耐药严重限制了长期疗效,成为肿瘤复发与转移的关键临床瓶颈。因此,探索新型治疗靶点及开发更有效的干预策略具有重要临床意义。
近期发表于《Jeju Journal of Island Sciences》的一项研究,揭示了MEK1/2抑制剂曲美替尼(Trametinib)对ER+乳腺癌细胞中ETV4表达的调控机制及其抗肿瘤效应。研究者利用CellCyte X活细胞成像系统,在2D及3D培养的MCF-7细胞模型中实现实时动态监测,确证曲美替尼可显著抑制细胞增殖。研究结果为 ETV4 作为 ER+乳腺癌潜在治疗靶点提供了新的实验证据,也为采用 MEK 抑制剂靶向 ETV4 以克服内分泌治疗耐药提供了理论基础。

材料与方法
1. 细胞培养与耐药株构建
MCF-7 细胞培养于含 10% 胎牛血清、100 U/mL 青霉素与100 μg/mL 链霉素的 DMEM 培养基,培养条件为 37℃、5% CO₂。他莫昔芬耐药 MCF-7(TAM-R_MCF-7)细胞参照文献构建:PBS 洗涤后更换无酚红 DMEM,添加 10% 活性炭处理胎牛血清及 0.1 μM 4 - 羟基他莫昔芬,诱导 2 周后逐步提升药物浓度至 3 μM,全程约 9 个月。
2. 蛋白免疫印迹分析
细胞经PBS 洗涤后,以 RIPA 裂解液提取总蛋白,离心去除细胞碎片。蛋白样品经 SDS-PAGE 分离后转印至硝酸纤维素膜,依次孵育一抗及 HRP 标记二抗,采用 ECL 化学发光法显影,ChemiDoc 成像系统(Bio-Rad)采集信号。
3. 报告基因实验
采用双荧光素酶报告基因系统检测ETV4启动子活性。MCF-7、T47D、BT474细胞以1×10⁵个/孔接种于12孔板,过夜培养后使用Fugene6试剂瞬时转染含ETV4启动子-RenSP的质粒。细胞在含/不含1 μM曲美替尼的培养基中培养24小时,使用发光仪(Tecan)检测海肾荧光素酶活性。
4. 2D细胞增殖实验
MCF-7细胞以2×10³个/孔接种于96孔板,连续培养 96 h。使用CellCyte X活细胞成像系统自动采集图像,设定时间点为0、24、48、72、96小时。通过CellCyte X软件内置分析模块完成细胞区域分割,以细胞覆盖面积定量分析不同浓度曲美替尼的增殖抑制作用。
5. 3D球体生长实验与大小评估
MCF-7细胞以3×10³个/孔接种于超低吸附96孔板,300×g离心3分钟促进细胞聚集。24h后加入含不同浓度(0.001、0.01、0.1 μM)曲美替尼的培养基,每24h采集图像。使用CellCyte X软件测量球体周长,评估药物对3D细胞生长的抑制作用。实验重复两次,每组设3个复孔。
6. 统计学分析
所有实验至少重复三次,数据以均值±标准差表示。使用GraphPad Prism 8软件进行单因素方差分析,以P<0.05为差异具有统计学意义。
实验结果
1. MAPK 信号通路调控 ER+乳腺癌细胞中 ETV4 的表达
已有研究证实,丝裂原活化蛋白激酶(MAPK)信号通路可通过磷酸化作用上调ETV4表达并增强其转录活性。为验证该调控机制在ER+乳腺癌中同样存在,本研究使用 MEK1/2 抑制剂曲美替尼处理 MCF-7 细胞。结果显示,曲美替尼显著降低ERK1/2 Thr202/Tyr204位点磷酸化水平(p<0.01),证实MEK1/2活性被有效抑制;Western blot检测显示ETV4蛋白表达呈剂量依赖性下降,这表明MAPK通路直接调控ER+乳腺癌细胞中ETV4的表达。
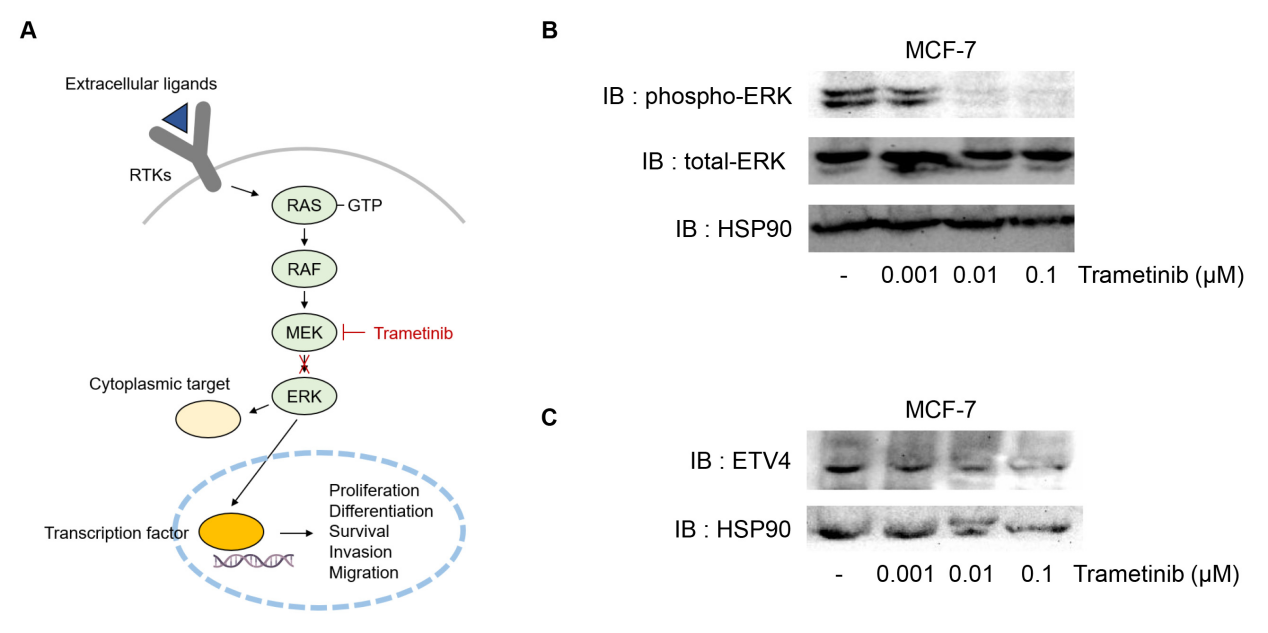
图 1. 曲美替尼对 MCF-7 细胞中 MAPK 信号下游效应因子 ETV4 的影响
2. 曲美替尼在转录水平抑制 ETV4 表达
为深入探究曲美替尼(Trametinib)下调ETV4的分子机制,本研究采用ETV4启动子荧光素酶报告质粒检测其转录活性。结果显示:在三种ER+乳腺癌细胞系(MCF-7、T47D、BT474)中,经1 μM曲美替尼处理24小时后,ETV4启动子活性均显著降低(p<0.001)。该结果证实曲美替尼在转录水平直接抑制ETV4表达。
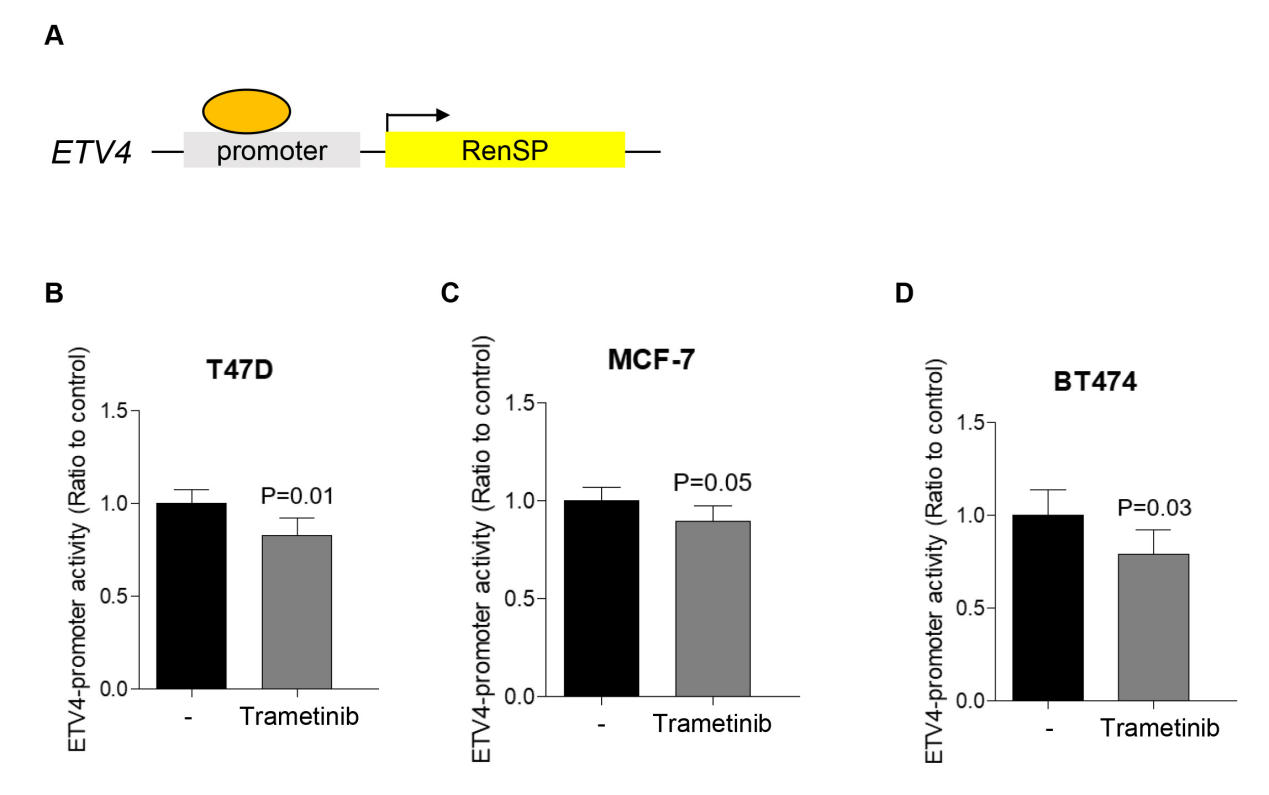
图 2. 曲美替尼对 ETV4 的转录调控作用
3. 曲美替尼在 2D 与 3D 模型中均抑制乳腺癌细胞生长
通过CellCyte X活细胞动态成像系统观测发现:在2D培养体系中,曲美替尼对MCF-7细胞增殖呈现剂量依赖性抑制,细胞覆盖面积较对照组显著降低。为模拟体内肿瘤微环境复杂性,本研究采用3D肿瘤球体模型。结果显示曲美替尼同样可显著抑制球体增长,表现出稳定的抗增殖效应。上述结果证实,曲美替尼在 2D 单层细胞及 3D 球体模型中均具有一致的抑瘤活性,不受细胞间相互作用及微环境异质性的影响。
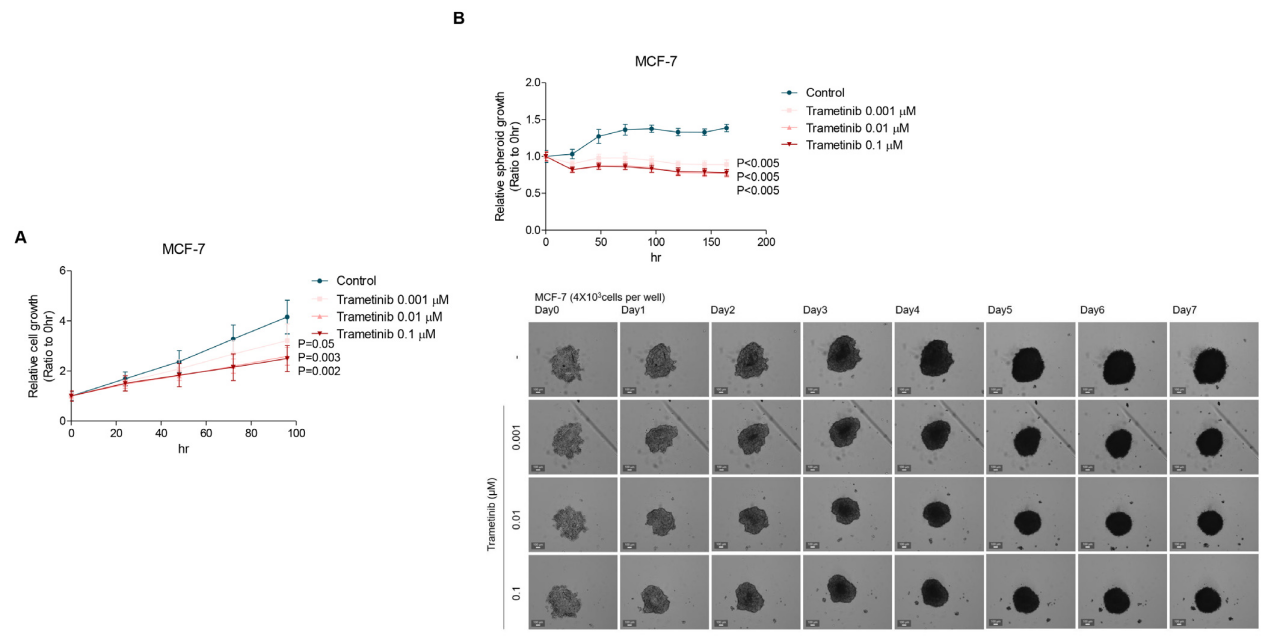
图 3. 曲美替尼对 MCF-7 细胞 2D 增殖及 3D 球体生长的抑制作用
4. ETV4 在他莫昔芬耐药细胞中表达显著上调
与亲本 MCF-7 细胞相比,TAM-R_MCF-7 细胞中 ETV4 的蛋白水平与 mRNA 水平均明显升高,提示 ETV4 异常上调可能他莫昔芬耐药的发生发展有关,为后续靶向 ETV4 逆转耐药提供了实验依据。
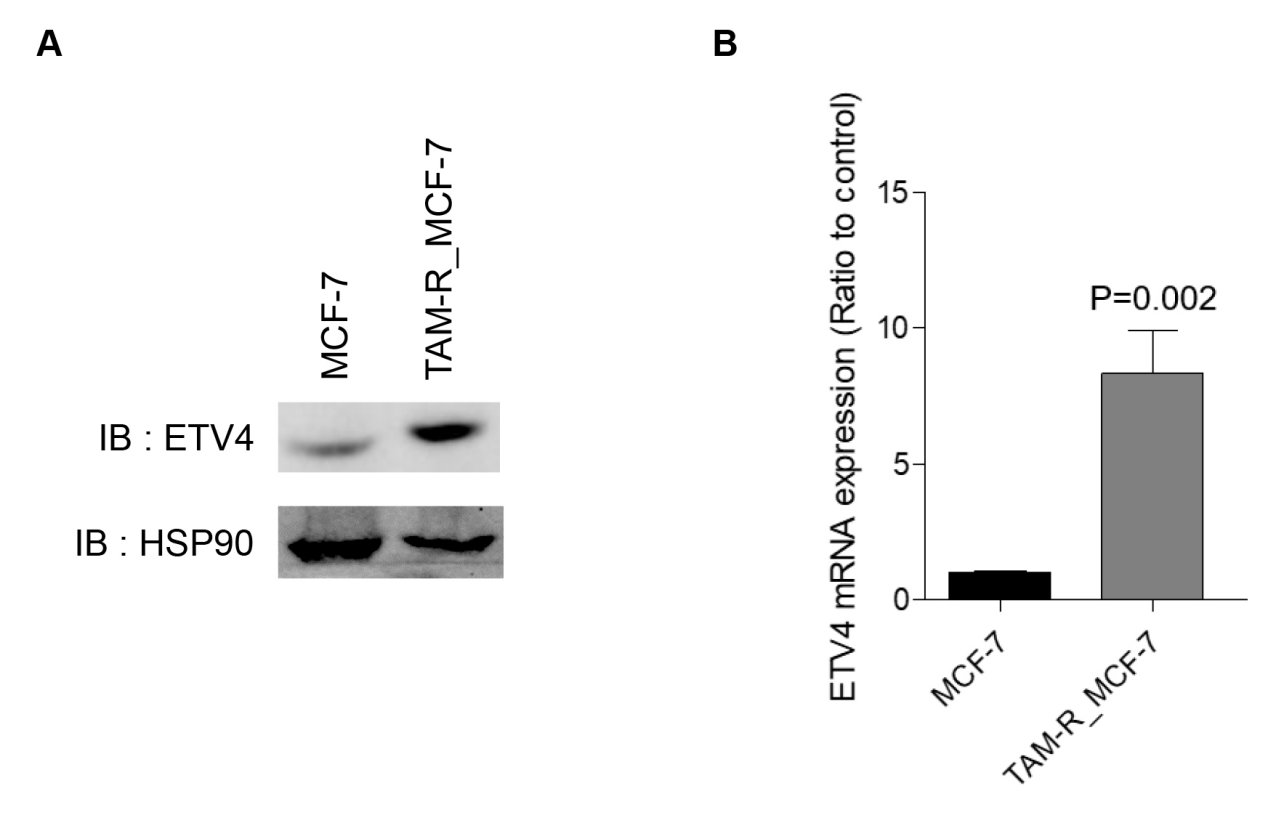
图 4. 与亲本 MCF-7 细胞相比,TAM-R_MCF-7 细胞中 ETV4 表达升高
5. MAPK-ETV4 轴驱动耐药细胞的增殖
TAM-R_MCF-7 细胞增殖速率显著高于亲本细胞,表现出更强的恶性表型。结合上述结果推测:在 ER+乳腺癌进展及耐药过程中,MAPK 信号异常激活可转录上调 ETV4,进而促进肿瘤细胞快速增殖。曲美替尼可通过阻断 MAPKETV4 信号轴,成为克服他莫昔芬耐药的潜在策略。
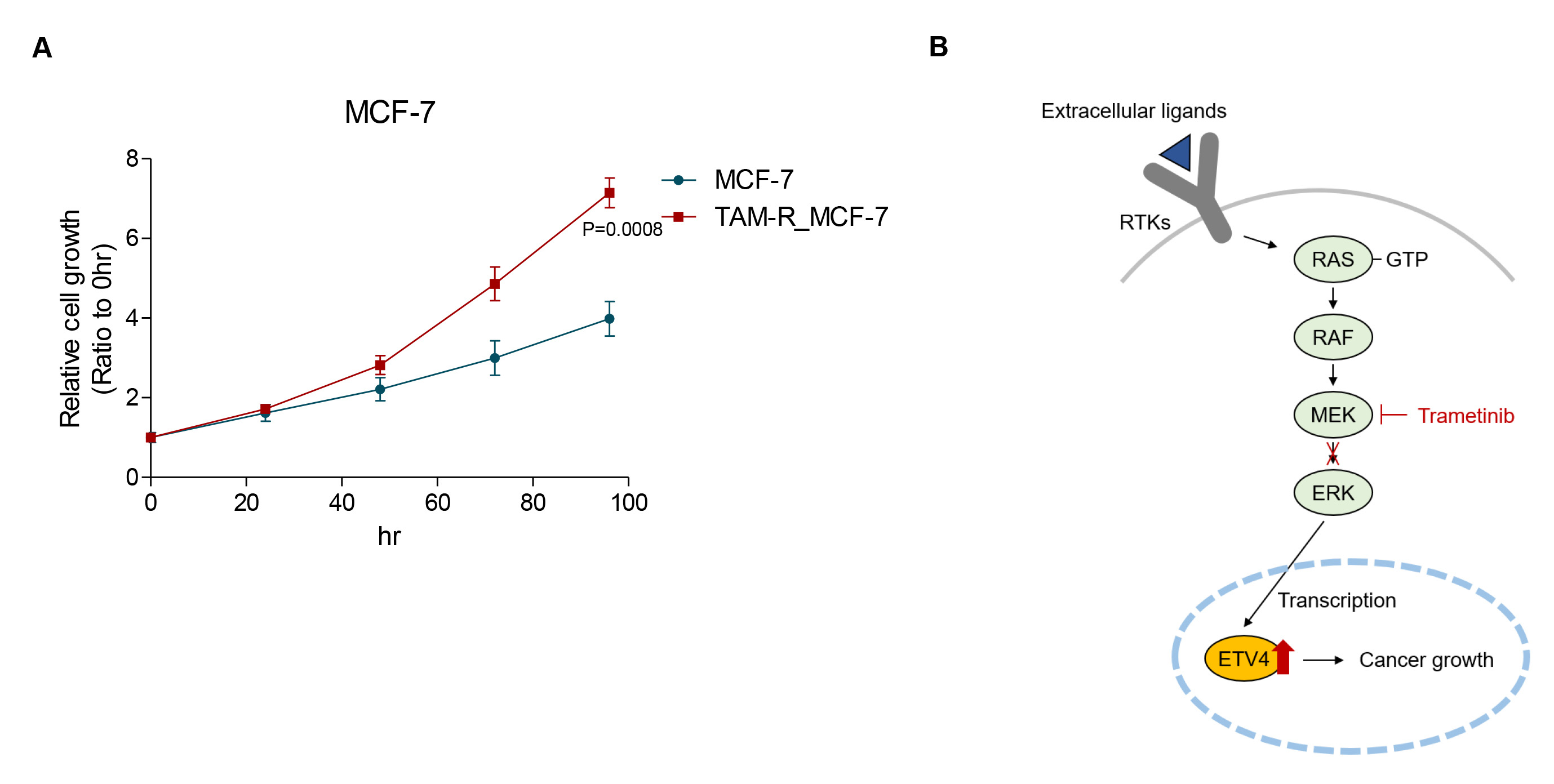
图 5. 与亲本 MCF-7 细胞相比,TAM-R_MCF-7 增殖能力显著增强
CellCyte X 技术优势
本研究充分体现了CellCyte X活细胞成像系统在抗肿瘤药物体外评价中的主要优势:
自动化成像,降低人为误差:系统可预设长期成像方案,实现多孔板高通量、连续无扰成像,保证数据采集的一致性与重复性,显著减轻实验人员操作负担。
精准图像分析,支持定量研究:软件内置分析模块可自动完成细胞覆盖面积、球体直径 / 周长等指标识别与量化,输出标准化、可追溯数据,提升实验结果可靠性与说服力。
兼容多体系培养模型:系统适配常规贴壁培养板与超低吸附 3D 培养板,可支持 2D 增殖、3D 肿瘤球体、细胞共培养等多种模型,满足体外肿瘤研究多样化需求。
这些功能使CellCyte X成为肿瘤药物筛选、机制研究、耐药模型构建等领域的理想工具。
应用前景与总结
本研究借助CellCyte X 活细胞成像系统,实时动态监测并定量评估了 MEK1/2 抑制剂曲美替尼对 ER+乳腺癌 MCF-7 细胞的增殖抑制效应,证实其在 2D 与 3D 培养体系中均具有稳定、一致的抗肿瘤活性,并进一步阐明了 ETV4 作为乳腺癌潜在治疗靶点的临床价值。
CellCyte X 系统凭借其自动化操作、高精度分析及多模型适配能力,为肿瘤生物学及药物筛选研究提供了高效、可靠的技术平台。在精准医学和新型抗肿瘤药物快速发展的背景下,该技术有望加速基础研究向临床转化,推动个体化治疗策略的优化与落地。




