2026.03.13
结直肠癌作为转移风险第二高的恶性肿瘤,在西方人群中发病率居高不下。其致命威胁主要源自循环肿瘤细胞(CTCs)形成的远处转移灶,这些具有异常表型的细胞群体直接导致了约20%的结直肠癌相关死亡。研究表明,此类肿瘤细胞常伴有CD44等表面标志物的高表达现象,同时其形态特征的细微变化与侵袭性增强和不良预后呈现密切关联。
近期发表于《Photonics》期刊的一项新研究,创新性地运用数字全息细胞术HoloMonitor M4系统,对三种转移性与两种非转移性结直肠癌细胞系开展了深入的形态学分析。该研究通过构建涵盖细胞面积、厚度、体积及不规则度的多参数识别体系,成功实现了癌细胞与外周血单个核细胞(PBMCs)的精确区分。令人瞩目的是,即便在癌细胞占比低至5%的混合样本中,该技术仍展现出强大的识别效能,可实现两类细胞的准确区分。
这一重要进展充分证实了数字全息细胞术作为高效、无标记新型检测工具的巨大潜力,特别适用于悬浮体系中不同尺寸细胞的精准鉴别。更重要的是,该技术具备与生物标志物检测联用的广阔前景,为结直肠癌相关循环肿瘤细胞(CTCs)的检测研究提供了新的技术思路。

图1. HoloMonitor M4
数字全息细胞术:无标记细胞分析的新兴工具
数字全息细胞术(Digital Holographic Cytometry, DHC)是一种基于定量相位成像(QPI)的先进活细胞分析技术。该技术通过记录激光穿透细胞时产生的全息图像,重建出细胞的三维形态与光学厚度分布,从而能够对细胞体积、面积、厚度及不规则度等多项形态参数进行高精度、非侵入式的测量。
与传统依赖染色或标记的荧光显微术相比,DHC无需任何标记处理,从根本上避免了荧光标记可能带来的光毒性和光漂白干扰,支持对活细胞进行长时间动态观测。这一特性使其在分析循环肿瘤细胞(CTCs)等脆弱且稀有的细胞类型时,展现出显著优势。
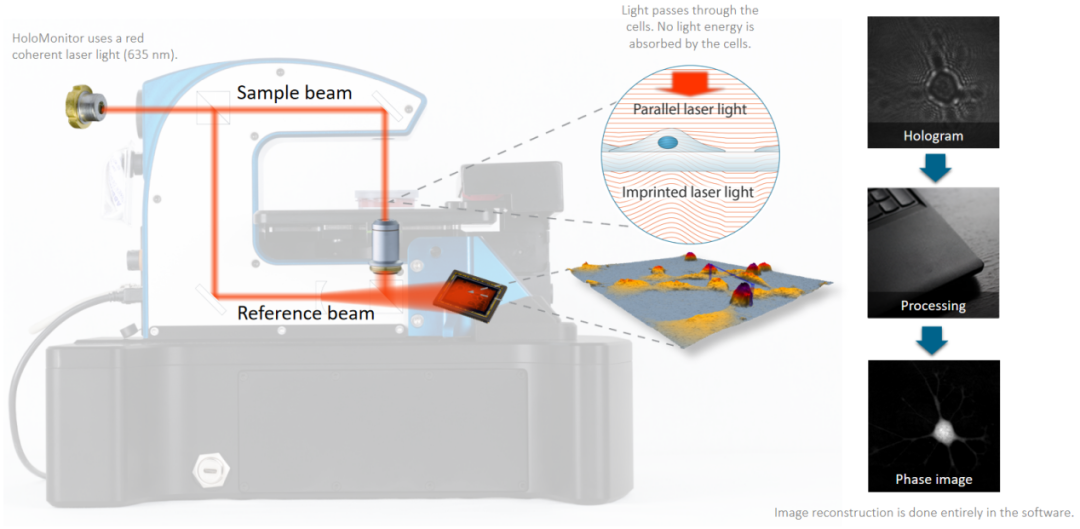
图2. HoloMonitor原理图示
技术路径与实验设计
研究团队采用 HoloMonitor M4 系统结合配套软件AppSuite 进行数字全息细胞术(DHC)分析,实现自动化细胞分割及形态参数提取。实验主要分为三个阶段:
1. 单一细胞系形态分析
对五种结直肠癌细胞系(COLO 205、Caco-2、NCI-H508、LS411N、SNU-C1)、MCF7乳腺癌细胞及外周血单个核细胞(PBMCs)分别进行单独培养与DHC分析,获取各类细胞在面积、厚度、体积及不规则度等方面的形态学基础数据。初步结果表明,COLO 205细胞与PBMCs的形态特征最为接近,因此选定该细胞系用于后续混合模型研究。
2. 混合细胞模型分析
为验证DHC在低丰度条件下的检测能力,研究将COLO 205细胞与PBMCs按设定比例(如10:90、5:95)混合,模拟循环肿瘤细胞(CTCs)在血液中的稀有状态。通过DHC实时成像与形态参数分析,系统评估该技术对少量癌细胞的识别与区分效能。
3. 分子标志物验证
为进一步确认细胞身份并探究上皮-间质转化(EMT)状态,研究辅以流式细胞术对上皮标志物EpCAM及间质标志物CD44进行检测,从而与形态学分析结果相互印证。
关键发现与结果
1. 细胞形态参数存在显著差异
尽管 COLO 205 细胞与 PBMCs 的形态较为接近,但数字全息细胞术(DHC)分析显示,前者的平均细胞面积(162.7 µm² vs 36.5 µm²)和平均光学厚度(8.8 µm vs 4.1 µm)均显著高于 PBMCs。其他结直肠癌细胞系(如 Caco-2、SNU-C1)在体积和面积上差异更为明显(图3)。
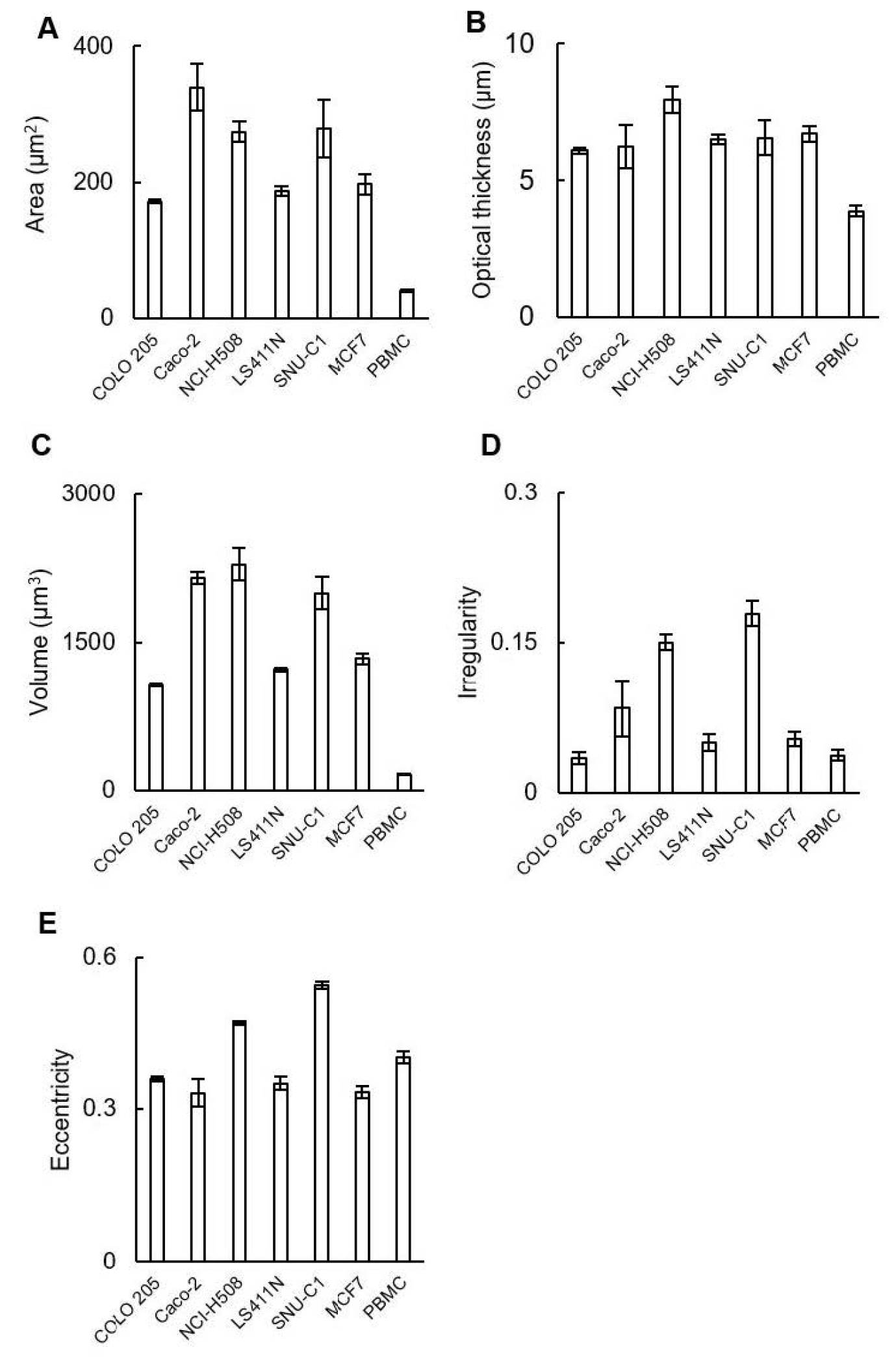
图3. 五种结直肠癌细胞系、MCF7细胞系及PBMCs的形态学参数分析
2. 低丰度混合条件下仍可高效识别
在 COLO 205 细胞仅占 5% 的混合样本中,DHC 技术仍能准确识别并区分两类细胞,检测准确率与预设的细胞比例高度一致(图4)。
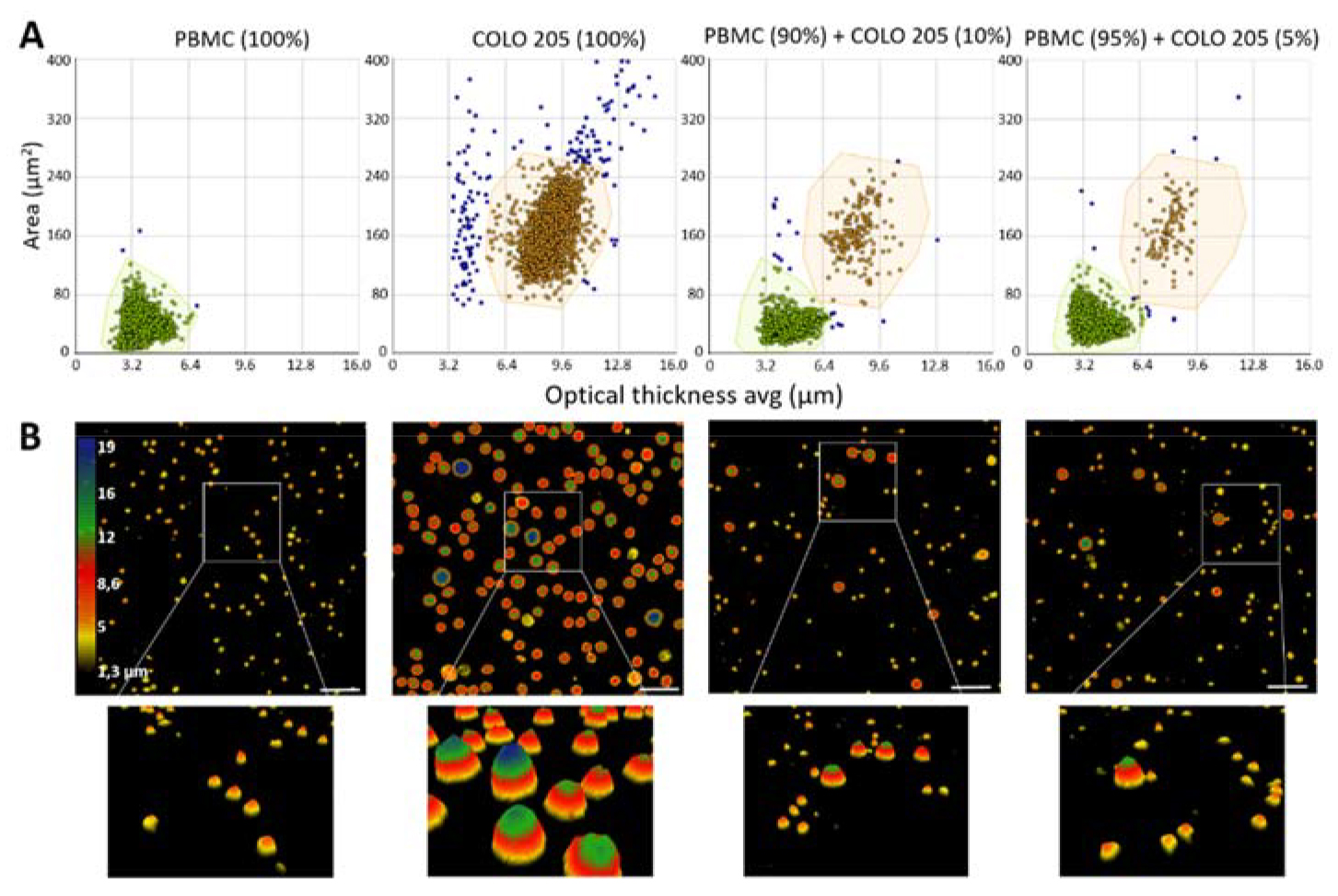
图4. PBMCs与COLO 205细胞在单独及混合悬浮状态下的检测结果
3. 形态参数与分子标志物分析结果互补
流式细胞术结果显示,COLO 205细胞高表达上皮标志物EpCAM而低表达间质标志物CD44,PBMCs的表达模式则恰恰相反。这一发现表明,将形态学分析与分子标志物检测相结合,能够更全面地表征细胞类型及其功能状态(图5)。
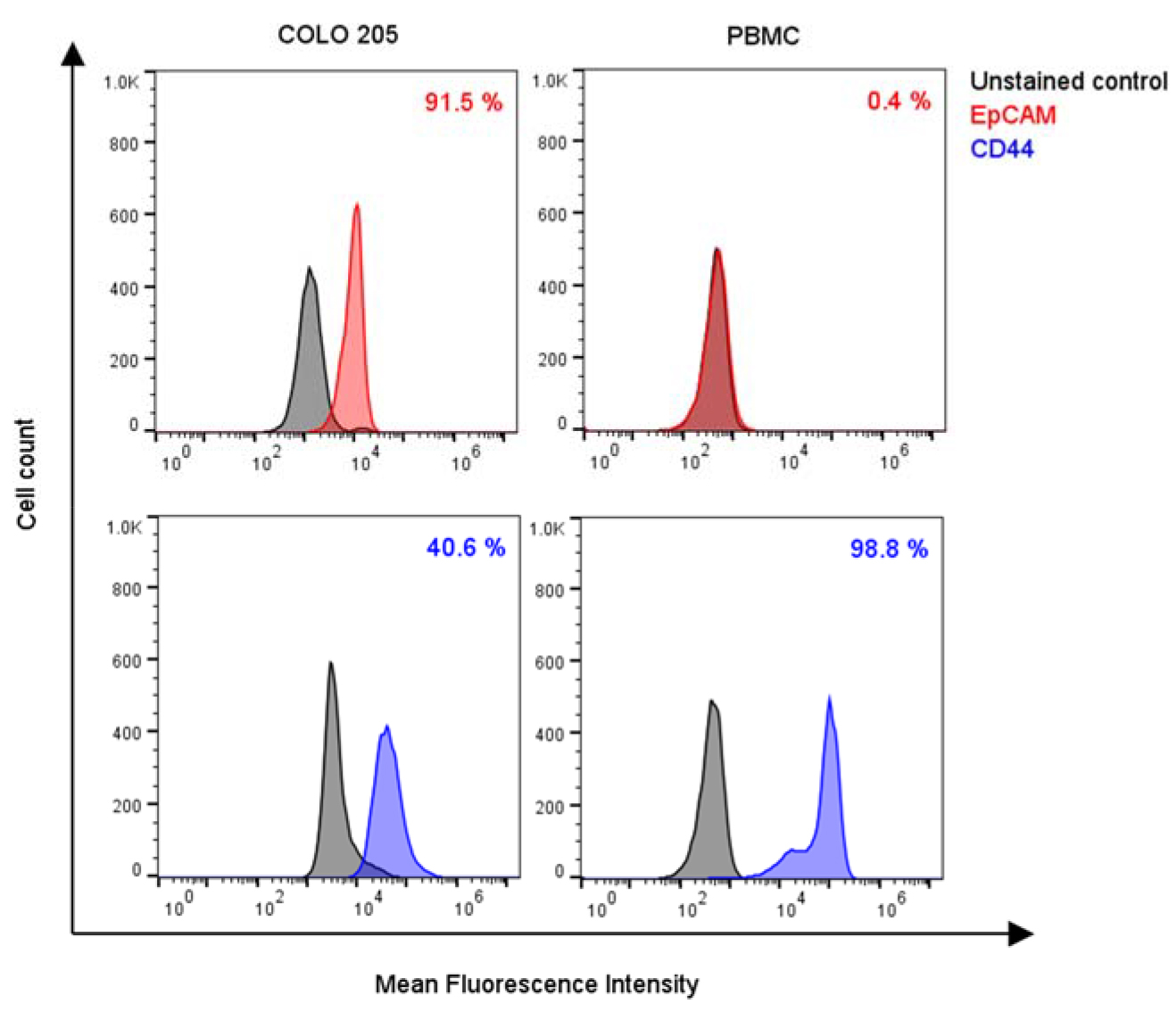
图5. COLO 205细胞与PBMCs的EpCAM和CD44表达情况
HoloMonitor技术优势与应用价值
本案例展示了HoloMonitor数字全息细胞术在循环肿瘤细胞(CTC)研究中的显著技术优势:
无标记与非侵入性:无需染色或标记,更大程度保持细胞原生状态,支持对活细胞进行长期、动态的观察。
高通量与多参数分析:单次扫描即可同时获取数十项细胞形态参数,显著提升分析效率与数据丰富度。
高灵敏度与特异性:即使在CTC占比很低(如5%)的复杂细胞混合样本中,仍能实现准确识别与区分。
良好的技术兼容性:可与微流控、荧光成像等平台相结合,构建多维、高内涵的细胞分析体系。
在临床应用层面,该技术在体外细胞检测领域的应用,或可为液体活检相关研究提供新的参考方向。为实现CTC的快速筛查、癌症早期诊断、疗效评估及复发监测提供有力工具。此外,其在药物筛选、细胞毒性评价、免疫细胞功能分析等研究领域也具有广泛的应用前景。
总结与展望
本研究通过建立体外循环肿瘤细胞(CTC)模型,证实了HoloMonitor数字全息细胞术可在无需标记的情况下,有效区分结直肠癌细胞与白细胞。该技术所具备的高精度形态分析能力,不仅为CTC检测提供了新的技术路径,也为肿瘤生物学研究提供了更接近体内真实环境的活细胞分析平台。
展望未来,随着人工智能与机器学习算法的进一步融合,HoloMonitor数字全息细胞术有望实现更智能化的细胞自动分类与病理诊断,从而为精准医疗的发展提供更强大的工具支持。
联系我们,获取 HoloMonitor 更多应用详情!




